Pin còn được viết theo tiếng Anh là "battery". Pin là một tập hợp của một hoặc nhiều tế bào mà các phản ứng hóa học của chúng tạo ra dòng electron trong mạch. Tất cả pin đều được tạo thành từ ba thành phần cơ bản: cực anode ('-' Pin), cực cathode ('+' Pin) và một số loại chất điện phân (chất phản ứng hóa học với cực anode và cực cathode).
1. Pin nó được làm như thế nào ?
Chúng ta không nên nhầm lẫn một “tế bào điện hóa” với một “tế bào điện phân” ở Hình 1-1. Tế bào điện hóa gồm hai điện cực ngăn cách nhau bằng bình điện phân. Tế bào điện phân được cung cấp bởi một nguồn điện bên ngoài để thúc đẩy quá trình điện phân. Do đó, một tế bào điện phân tiêu thụ điện, trong khi một tế bào điện hóa sản xuất ra điện.
2. Cấu tạo pin gồm những gì ?
Mũi tên màu cam đại diện cho các ion đồng dương. Các mũi tên màu trắng đại diện cho các ion kẽm dương. (Ion là nguyên tử có sự thừa hoặc thiếu electron.) Các ion kẽm bị hút vào chất điện phân kẽm sunfat, dẫn đến sự mất khối lượng thực từ điện cực kẽm.
Trong khi đó, các electron đi vào điện cực đồng có xu hướng nhận các ion đồng dương, được hiển thị dưới dạng mũi tên màu cam trong Hình 2-1. Các ion đồng được tách ra khỏi chất điện phân đồng sunfat, và dẫn đến sự tích tụ của các nguyên tử đồng trên điện cực đồng.
Quá trình này tạo thành năng lượng một phần bởi thực tế là kẽm có xu hướng cho electron dễ dàng hơn đồng.
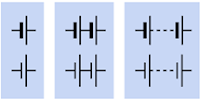
Pin sử dụng trong các thiết bị điện tử dân dụng, thường sử dụng chất dẻo thay vì chất lỏng làm chất điện phân, và được gọi là pin khô như trong pin kiềm 1,5 volt C, D, AA hoặc AAA điển hình (xem Hình 2-2).
3.Thuật ngữ điện cực là gì ?
Các điện cực của tế bào thường được gọi là cực dương và cực âm. Những thuật ngữ này thường “gây nhầm lẫn” nên cần lưu ý.
Dòng điện thông thường được tưởng tượng là chạy theo hướng ngược lại với các electron. Khi ở bên ngoài tế bào, dòng điện này chạy từ cực cathode (cực đồng) đến cực anode (cực kẽm), và từ quan điểm này, cực cathode có thể được coi là "dương hơn" so với cực anode. Để ghi nhớ điều này, hãy nghĩ về chữ t trong “cathode” là một dấu +. Vì vậy khi đo điện áp cực đồng sẽ dương hơn cực kẽm
4. Các loại pin
Có ba loại pin :
a. Pin dùng một lần: được gọi là pin (primary cells). Chúng không thể sạc lại được vì phản ứng hóa học không thể đảo ngược.
b. Pin có thể sạc lại: được gọi là pin (secondary cells). Chúng có thể được sạc lại bằng cách đặt một điện áp giữa hai đầu pin bằng nguồn điện bên ngoài chẳng hạn như bộ sạc pin. Các vật liệu được sử dụng trong pin và cách bảo quản pin, sẽ ảnh hưởng đến tốc độ suy thoái hóa học của các điện cực dần dần xảy ra khi nó được sạc lại nhiều lần. Dù bằng cách nào, thì số lần chu kỳ nạp / xả đều bị giới hạn.
c. Pin Nhiên liệu: được gọi là pin (Fuel Cells require). Chúng cần một luồng khí phản ứng như hydro để duy trì phản ứng điện hóa trong một thời gian dài.
Một pin nhiên liệu bao gồm một cực dương (fuel electrode), một cực âm (air electrode) và một chất điện phân dày đặc mà chỉ một số ion nhất định có thể di chuyển qua đó ( Hình 4-1). Với cấu trúc này, pin nhiên liệu tạo ra điện thông qua phản ứng giữa hydro trong nhiên liệu và oxy. Tại cực dương, hydro bị phân hủy thành các ion hydro và các electron. Khi một tải ngoài được nối giữa cực dương và cực âm, các electron chạy qua tải này. Trong khi đó, các ion hydro đi qua chất điện phân đến điện cực không khí, nơi chúng phản ứng với oxy và các electron được cung cấp từ mạch ngoài để tạo thành nước. Mỗi điện cực đóng một vai trò quan trọng trong sự khuếch tán khí giữa bề mặt, bề mặt điện cực và chất điện phân, nơi các phản ứng hóa học diễn ra. Vì lý do này, các điện cực thường được yêu cầu phải có cấu trúc xốp. Mặc dù ở đây chúng ta đã giả định rằng các ion dương (ion hydro) di chuyển trong chất điện phân, pin nhiên liệu trong đó các ion âm như ion oxy di chuyển.
5. Dung lượng của pin.
Dung lương của pin được đo bằng amp-giờ, viết tắt là Ah, AH.. Các giá trị nhỏ hơn được đo bằng miliamp giờ, thường được viết tắt là mAh. Nếu I là dòng điện được tạo ra từ pin (tính bằng ampe) và T là thời gian pin có thể cung cấp dòng điện đó (tính bằng giờ), thì dung lượng amp giờ được tính theo công thức:
Ah = I * T
Bằng cách thay đổi công thức, nếu chúng ta biết dung lượng amp giờ của pin mà nhà sản xuất đã cho, chúng ta có thể tính được thời gian sử dụng mà pin có thể cung cấp một dòng điện cụ thể:
T = Ah / I
Ví dụ :
Về mặt lý thuyết, Ah là một giá trị không đổi đối với bất kỳ loại pin nào. Do đó, với pin được có dung lượng 4Ah sẽ cung cấp dòng điện 1 amp trong 4 giờ.
Lúc này ta sử dụng dòng điện 4 ampe trong 1 giờ sẽ hết pin, khi ta muốn sừ dụng với dòng 5 ampe thì pin sẽ hết trong 0,8 giờ (0,8*60 = 48 phút),...
Trong thực tế, mối quan hệ này không tồn tại. Nó nhanh chóng bị hỏng khi dòng điện tăng lên, đặc biệt là khi sử dụng pin axit-chì, loại pin này không hoạt động tốt khi được yêu cầu cung cấp dòng điện cao. Một phần dòng điện bị mất dưới dạng nhiệt và pin có thể không đủ khả năng điện hóa để đáp ứng nhu cầu.
6. Điện áp của pin.
Điện áp danh định của pin đã sạc đầy được gọi là điện áp hở mạch (viết tắt là OCV hoặc Voc), được định nghĩa là điện thế tồn tại khi không có tải nào được đặt giữa các cực.
Vì nội trở bên trong của đồng hồ đo vôn (hoặc đồng hồ vạn năng, khi nó được sử dụng để đo volt DC) rất cao, nên nó có thể được kết nối trực tiếp giữa các cực của pin với dòng không tải , và sẽ hiển thị OCV khá chính xác, nên không thể làm hỏng đồng hồ. Pin ô tô 12 volt được sạc đầy có thể có OCV khoảng 12,6 volt, trong khi pin kiềm 9 volt mới thường có OCV khoảng 9,5 volt.
7. Chọn pin khi sử dụng.
Khi chọn pin để cung cấp cho mạch, ta cần quan tâm thời gian sử dụng dự kiến, mức tiêu hao dòng điện tối đa và đặc biệt là dung lượng pin.
Đối với các mạch 5V sử dụng nguồn điện từ 100mA trở xuống, người ta thường sử dụng pin 9V hoặc sáu pin 1,5V mắc nối tiếp, cho dòng điện đi qua bộ IC ổn áp như LM7805. Lưu ý rằng bộ điều chỉnh điện áp (LM7805) yêu cầu điện áp để hoạt động, và do đó một điện áp thả xuống GND sẽ bị tiêu tán dưới dạng nhiệt.